1.O modelo de átomo proposto por Dalton, como uma esfera maciça e indivisível, não corresponde ao que é válido atualmente. Explique por que a comunidade científica da época de Dalton o aceitava. (1,0)
__________________________________________________________________________________________________________________________________________________________________________________________________________________
2.Observe este esquema de um átomo neutro de sódio:
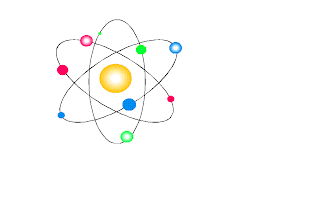
a)Identifique a região do átomo apontada pela cor amarela.
____________________________________________________________________________________
b)Qual o nome da partícula subatômica apontada pela cor verde? Sua carga elétrica é positiva ou negativa?
_________________________________________________________________________________________________________________________________________________________________________
c)Qual o número de prótons desse átomo? Justifique sua resposta.
____________________________________________________________________________________
d)Qual o número atômico desse átomo? Justifique sua resposta.
__________________________________________________________________________________________________________________________________________________________________________
e) Sabendo que esse átomo tem 12 nêutrons, qual é seu número de massa? Por quê?
__________________________________________________________________________________________________________________________________________________________________________
f)Se esse átomo perder um elétron, ele continua eletricamente neutro. Como ele poderá ser então denominado?
__________________________________________________________________________________________________________________________________________________________________________
g)O átomo de sódio possui três camadas eletrônicas. Em qual delas a energia do elétron é maior?
__________________________________________________________________________________________________________________________________________________________________________
3.Uma estudante escreveu que toda a massa de um átomo está praticamente concentrada em seu núcleo. Você concorda? Por quê?
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
4.Faça a distribuição eletrônica em camadas dos átomos dos seguintes elementos:
a)Zinco (Z=30)
__________________________________________________________________________________________________________________________________________________________________________
b)Telúrio (Z=52)
__________________________________________________________________________________________________________________________________________________________________________
c)Enxofre (Z=16)
__________________________________________________________________________________________________________________________________________________________________________
d)Alumínio (Z=13)
__________________________________________________________________________________________________________________________________________________________________________
5.Verifique se as afirmativas abaixo estão corretas. Caso não estejam, reescreva-as no caderno fazendo as correções necessárias. Se estiverem corretas explique por quê.
a)Isótopos são átomos que apresentam o mesmo número atômico e o mesmo número de massa.
__________________________________________________________________________________________________________________________________________________________________________
b)Constituem um elemento químico apenas os átomos que têm o mesmo Z e o mesmo Z.
__________________________________________________________________________________________________________________________________________________________________________
c)O átomo constituído de 17 prótons, 18 nêutrons e 17 elétrons apresenta Z=17 e A=35.
__________________________________________________________________________________________________________________________________________________________________________
6.Reescreva as afirmativas corrigindo-as.
a)Quando se compara o átomo neutro de enxofre (S) como íon sulfeto (S2-), verifica-se que este tem dois prótons a mais e o mesmo número de elétrons.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
b)Sabemos que o número atômico do chumbo (Pb) é igual a 82 e que o íon Pb2+ apresenta 127 nêutrons. Concluímos, portanto, que o número de elétrons ao redor do núcleo do íon é igual a 82.
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
7.Estabeleça as diferenças entre grupo e período na tabela periódica.
__________________________________________________________________________________________________________________________________________________________________________
8.Dê o nome e o símbolo de:
a)Três elementos químicos classificados como metais.
__________________________________________________________________________________________________________________________________________________________________________
b)Quatro elementos químicos classificados como não-metais.
__________________________________________________________________________________________________________________________________________________________________________
9.Nomeie e dê o símbolo de três metais de transição do quarto período.
__________________________________________________________________________________________________________________________________________________________________________
10.Para cada metal nomeado, faça uma lista de alguns de seus usos (pesquise em dicionários, enciclopédias ou na Internet). Não se esqueça de indicar a fonte de consulta.
__________________________________________________________________________________________________________________________________________________________________________
